Phản ứng oxi hoá khử là một trong những quá trình quan trọng nhất của thiên nhiên. Sự hô hấp, quá trình thực vật hấp thụ khí cacbonic giải phóng oxi, sự trao đổi chất và hàng loạt quá trình sinh học khá đều có cơ sở là phản ứng oxi hoá – khử. Sự đốt cháy nhiên liệu trong các động cơ, các quá trình điện phân, các phản ứng xảy ra trong pin, acquy đều bao gồm sự oxi hoá và sự khử. Hàng loạt quá trình sản xuất như luyện kim, chế tạo hoá chất, chất dẻo, dược phẩm, phân bón hoá học… đều không thực hiện được nếu thiếu các phản ứng oxi hoá khử.

Trong hoá học, phản ứng oxi hoá – khử cũng chiếm vai trò rất quan trọng. Trong bài viết này, chúng ta sẽ tìm hiểu các vấn đề lí thuyết có liên quan đến loại phản ứng này.
KHÁI NIỆM PHẢN ỨNG OXI HÓA KHỬ
1. Phản ứng oxi hoá – khử
– Khái niệm: Phản ứng oxi hóa – khử là phản ứng hoá học trong đó có sự chuyển e giữa các chất phản ứng.
– Dấu hiệu nhận biết: Phản ứng có sự thay đổi số oxi hóa của một số nguyên tố.
2. Chất khử (chất bị oxi hoá)
– Khái niệm: Chất khử là chất có khả năng nhường e (cho e).
– Dấu hiệu nhận biêt:
+ Sau phản ứng, số oxi hoá của chất khử tăng.
+ Chất khử có chứa nguyên tố chưa đạt đến mức oxi hoá cao nhất.
Chú ý: Nguyên tố ở nhóm XA có số oxi hoá cao nhất là +X.
3. Chất oxi hoá (chất bị khử)
– Khái niệm: Chất oxi hoá là chất có khả năng nhận e (thu e).
– Dấu hiệu:
+ Sau phản ứng, số oxi hoá của chất oxi hoá giảm.
+ Chất oxi hoá có chứa nguyên tố có mức oxi hoá chưa phải thấp nhất.
Chú ý: Kim loại có số oxi hoá thấp nhất là 0, phi kim thuộc nhóm xA thì số oxi hoá thấp nhất là (x – 8).
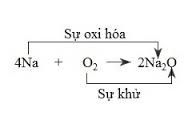
4. Sự khử và sự oxi hoá
– Sự khử (quá trình khử) của một chất là làm cho chất đó nhận electron hay làm giảm số oxi hoá của chất đó.
– Sự oxi hoá (quá trình oxi hoá) của một chất là làm cho chất đó nhường electron hay làm tăng số oxi hoá của chất đó.
ĐIỀU KIỆN CỦA PHẢN ỨNG OXI HOÁ KHỬ
Phải có sự tham gia đồng thời của chất khử và chất oxi hóa. Chất khử và chất oxi hóa phải đủ mạnh.
PHÂN LOẠI PHẢN ỨNG OXI HOÁ KHỬ
Phản ứng oxi hoá – khử được chia thành nhiều loại khác nhau:
– Phản ứng oxi hóa – khử thông thường: chất khử và chất oxi hóa ở 2 phân tử chất khác nhau.
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O
Cu + 2H2SO4 đặc → CuSO4 + SO2 + 2H2O
– Phản ứng oxi hóa – khử nội phân tử: chất khử và chất oxi hóa thuộc cùng 1 phân tử nhưng ở 2 nguyên tử khác nhau (thường gặp là phản ứng nhiệt phân).
AgNO3 → Ag + NO2 + O2
Cu(NO3)2 → CuO + NO2 + O2
– Phản ứng tự oxi hóa – khử, chất khử đồng thời cũng là chất oxi hóa (chất khử và chất oxi hoá thuộc về cùng một nguyên tố trong một phân tử chất).
Cl2 + 2NaOH → NaCl + NaClO + H2O
2NO2 + 2NaOH → NaNO2 + NaNO3 + H2O
4KClO3 → 3KClO4 + KCl