TÍNH CHẤT VẬT LÝ ancol

– Ancol có nhiệt độ nóng chảy, nhiệt độ sôi và độ tan trong nước cao hơn so với hiđrocacbon, dẫn xuất halogen, ete có khối lượng phân tử tương tự.
Nguyên nhân: ancol có liên kết –O–H phân cực nên hình thành được liên kết hiđro với nhau (làm tăng nhiệt độ nóng chảy, nhiệt độ sôi) và với nước (làm tăng độ tan trong nước).
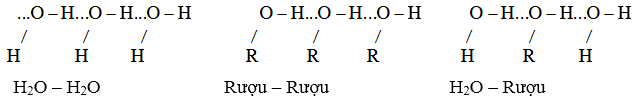
1. Trạng thái của ancol
– Từ C1 đến C12 là chất lỏng, từ C13 trở lên là chất rắn.
2. Nhiệt độ sôi của ancol
– So với các chất có M tương đương thì nhiệt độ sôi của: Muối > Axit > Ancol > Anđehit > Hiđrocacbon, ete và este…
– Giải thích: nhiệt độ sôi của một chất thường phụ thuộc vào các yếu tố:
+ M: M càng lớn thì nhiệt độ sôi càng cao.
+ Độ phân cực của liên kết: liên kết ion > liên kết cộng hóa trị có cực > liên kết cộng hóa trị không cực.
+ Số liên kết hiđro: càng nhiều liên kết H thì nhiệt độ sôi càng cao.
+ Độ bền của liên kết hiđro: liên kết H càng bền thì nhiệt độ sôi càng cao.
3. Độ tan của ancol
– Ancol có 1, 2, 3 nguyên tử C trong phân tử tan vô hạn trong nước.
– Ancol có càng nhiều C, độ tan trong nước càng giảm vì tính kị nước của gốc hiđrocacbon tăng.
V. Điều chế Ancol
1. Thủy phân dẫn xuất halogen
CnH2n+2-2k-xXx + xMOH → CnH2n+2-2k-x(OH)x + xMX
2. Cộng nước vào anken tạo ancol no, đơn chức, mạch hở
CnH2n + H2O → CnH2n+1OH (H+)
Phản ứng tuân theo quy tắc cộng Maccopnhicop nên nếu anken đối xứng thì phản ứng chỉ tạo thành 1 ancol.
3. Thủy phân este trong môi trường kiềm
RCOOR’ + NaOH → RCOONa + R’OH
4. Cộng H2 vào anđehit hoặc xeton
RCHO + H2 → RCH2OH (Ni, t0)
RCOR’ + H2 → RCHOHR’ (Ni, t0)
5. Oxi hóa hợp chất có nối đôi bằng dung dịch KMnO4
3CH2=CH2 + 2KMnO4 + 4H2O → 3CH2OH-CH2OH + 2KOH + 2MnO2
6. Phương pháp riêng điều chế CH3OH
CH4 + H2O → CO + 3H2
CO + 2H2 → CH3OH (ZnO, CrO3, 4000C, 200atm)
2CH4 + O2 → 2 CH3OH (Cu, 2000C, 100 atm)
7. Phương pháp điều chế C2H5OH
– Lên men tinh bột:
(C6H10O5)n → C6H12O6 → C2H5OH
– Các phản ứng cụ thể:
(C6H10O5)n + nH2O → nC6H12O6
C6H12O6 → 2C2H5OH + 2CO2 (men rượu)
– Hidrat hóa etilen, xúc tác axit:
C2H4 + H2O → C2H5OH
– Đây là các phương pháp điều chế ancol etylic trong công nghiệp.
V. Cách nhận biết Ancol
– Ancol tạo khí không màu với kim loại kiềm (chú ý mọi dung dịch đều có phản ứng này).
– Ancol làm CuO đun nóng từ màu đen chuyển thành Cu màu đỏ.
– Ancol đa chức có các nhóm OH liền kề hòa tan Cu(OH)2 tạo dung dịch màu xanh.
– Ancol không no có phản ứng làm mất màu dung dịch Brom.
VI. Ứng dụng của ancol
– Metanol chủ yếu được dùng để sản xuất Andehit Fomic nguyên liệu cho công nghiệp chất dẻo.
– Etanol dùng để điều chế một số hợp chất hữu cơ như axit axetic, dietyl ete, etyl axetat,.. do có khả năng hòa tan tốt một số hợp chất hữu cơ nên Etanol được dùng để pha vecni, dược phẩm, nước hoa,…
– Trong đời sống hàng ngày Etanol được dùng để pha chế các loại đồ uống với độ ancol khác nhau.
