III. TÍNH CHẤT HÓA HỌC Akađien

1. Phản ứng cộng H2, cộng dung dịch Br2và cộng HX
Do mang liên kết đôi C=C trong phân tử nên ankađien cũng có phản ứng đặc trưng là phản ứng cộng. Vì có chứa 2 liên kêt đôi C=C nên ankađien có thể tham gia phản ứng cộng theo tỉ lệ mol 1 : 1 hoặc 1 : 2.
a. Cộng tỉ lệ mol 1:1
– Cộng kiểu 1,2 (ở nhiệt độ thấp khoảng -800C): phản ứng này chỉ tác động đến 1 liên kết đôi C=C, liên kết còn lại giữ nguyên.
CH2=CH-CH=CH2 + H2 $\xrightarrow{Ni,\text{ }{{t}^{0}}}$ CH3-CH2-CH=CH2
– Cộng kiểu 1,4 (ở nhiệt độ cao hơn khoảng 400C): phản ứng này tác động đến cả 2 liên kết đôi và tạo ra 1 liên kết đôi C=C mới nằm giữa 2 liên kết đôi ban đầu.
CH2=CH-CH=CH2 + H2 $\xrightarrow{Ni,\text{ }{{t}^{0}}}$ CH3-CH=CH-CH3
– Buta−1,3−đien cũng như isopren có thể tham gia phản ứng cộng Cl2, Br2, HCl, HBr,… và thường tạo thành hỗn hợp các sản phẩm theo kiểu cộng 1,2 và cộng 1,4.
– Ở nhiệt độ thấp thì ưu tiên tạo thành sản phẩm cộng 1,2; ở nhiệt độ cao thì ưu tiên tạo ra sản phẩm cộng 1,4
Ví dụ: isopren phản ứng với brom theo tỉ lệ 1 : 1
– Ở 40oC:
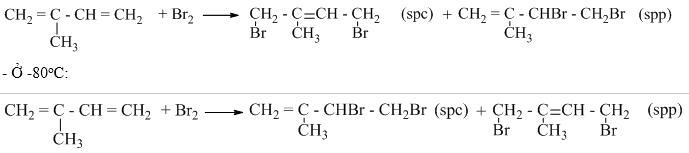
b. Cộng tỉ lệ mol 1:2
CH2=CH-CH=CH2 + 2H2 CH3-CH2-CH2-CH3
CH2=CH-CH=CH2 + 2Br2 → CH2Br-CHBr-CHBr-CH2Br
CH2=CH-CH=CH2 + HBr → hh sp: CH3-CHBr-CHBr-CH3 + CH3-CHBr-CH2-CH2Br + CH2Br-CH2-CH2-CH2Br
2. Phản ứng trùng hợp
Các phản ứng trùng hợp chủ yếu xảy ra theo kiểu 1,4.
nCH2=CH-CH=CH2 $\xrightarrow{Na,{{t}^{o}}}$ (-CH2-CH=CH-CH2-)n
(Cao su buna)
nCH2=C(CH3)-CH=CH2 $\xrightarrow{xt,{{t}^{o}},p}$ (-CH2-C(CH3)=CH-CH2-)n
(Cao su isopren)
3. Phản ứng oxi hóa
a. Oxi hóa hoàn toàn
${{C}_{n}}{{H}_{2n-2}}~+\text{ }\dfrac{3n-1}{2}{{O}_{2}}~\to ~nC{{O}_{2}}~+\text{ }\left( n-1 \right){{H}_{2}}O$
Đặc điểm của phản ứng đốt cháy ankađien: nCO2 > nH2O và nCO2 – nH2O = nankađien
b. Oxi hóa không hoàn toàn: Ankađien cũng làm mất màu dung dịch thuốc tím ở ngay nhiệt độ thường.