Nhóm Halogen và tính chất, hóa học phổ thông

Vị trí của đơn chất halogen trong bảng tuần hoàn
– Nhóm halogen: nhóm VIIA.
– Nhóm halogen: gồm Flo (F), Clo (Cl), Brom (Br) và Iot (I).
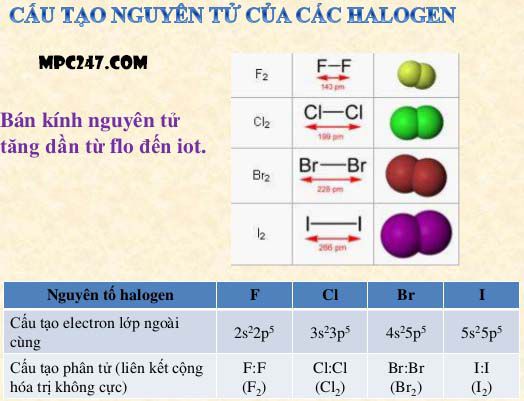
Một số đặc điểm của các halogen
Tính chất vật lí
– Trạng thái và màu sắc: Flo (khí, lục nhạt), Clo (khí, vàng lục), Brom (lỏng, đỏ nâu) và Iot (rắn, đen tím, dễ thăng hoa).
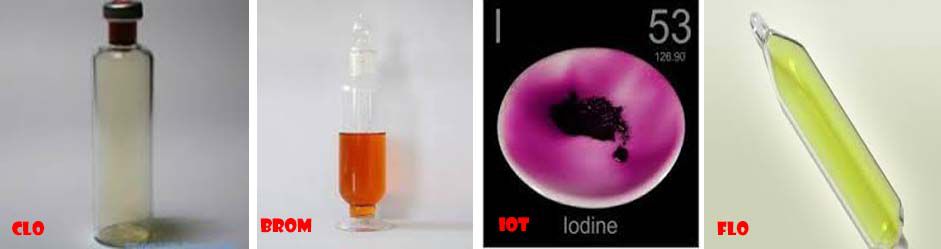
– Từ flo đến iot, nhiệt độ nóng chảy và nhiệt độ sôi tăng dần.
– Flo không tan trong nước, các halogen khác tan tương đối ít trong nước và tan nhiều trong một số dung môi hữu cơ.
Cấu hình e nguyên tử và cấu tạo phân tử của đơn chất halogen
– Cấu hình e lớp ngoài cùng: ns2np5.
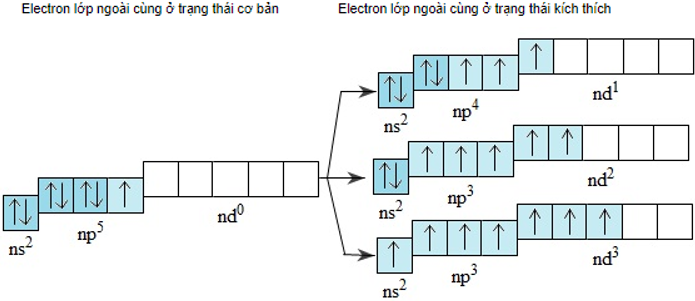
Cấu hình e ở trạng thái kích thích của Cl, Br và I
– Công thức đơn chất: X2: (F2, Cl2, Br2, I2).
– Cấu tạo phân tử: X – X. Liên kết trong phân tử đơn chất halogen là liên kết cộng hóa trị không phân cực.
Khái quát về tính chất hóa học của đơn chất halogen
– Do lớp e ngoài cùng đã có 7e nên halogen là những phi kim điển hình, dễ nhận thêm 1e thể hiện tính oxi hóa mạnh.
– Tính oxi hóa của các halogen giảm dần khi đi từ F2 đến I2.
– Trong các hợp chất, F chỉ có mức oxi hóa -1; các halogen khác ngoài mức oxi hóa -1 còn có mức +1; +3; +5; +7.
